新冠病毒德尔塔变异株的出现,造成全球疫情复燃。西安疫情的爆发,又引起一阵恐慌,这次疫情其更高的传播性与致病性让“现有疫苗是否能防范变异病毒”成为大家关注的热点,mRNA疫苗也一跃成为话题焦点。
我们目前知道的疫苗有减毒疫苗、灭活疫苗,代谢产物,其中代表产物的疫苗范围广,如重组蛋白疫苗也应该包括在内,以前听说过基因疫苗,随着时代发展,现在还有mRNA疫苗,高保护效力、良好的安全性和耐受性、强大的免疫原性以及更快的生产速度,使得mRNA疫苗从不同疫苗技术路线中脱颖而出。
mRNA疫苗是将编码疾病特异性抗原的mRNA引入体内,利用宿主细胞的蛋白质合成机制产生抗原,从而触发免疫应答。通常可根据不同疾病构建特异性抗原的mRNA序列,由新型脂质纳米载体颗粒包裹运送至细胞内,再利用人体核糖体翻译mRNA序列产生疾病的抗原蛋白,分泌后被自身免疫系统识别产生免疫反应,从而达到预防疾病作用。
虽然这些传统疫苗在许多疾病的预防上起到了重要作用,但是面对急性暴发的传染病,例如:此次的新型冠状病毒,传统疫苗的研发和生产周期是5-6个月,难以满足控制疫情的需要,因此我们需要更加有效、更加通用的疫苗开发平台,而mRNA疫苗就是破局的一个潜在方案。
早在1990年代,科学家将体外转录的mRNA注射到小鼠体内,发现其可在小鼠体内表达,产生相关蛋白且具有剂量依赖性,并能够诱导免疫反应,这也就是mRNA疫苗的雏形。当编码抗原蛋白的mRNA被注射进人体后,能够在体内合成抗原蛋白,从而引起人体免疫反应对抗病原体感染,即为mRNA疫苗。这类RNA疫苗能够在体内自我扩增,很少的量就可以引起较强的免疫反应。
非复制型的RNA疫苗,在体外转录好的一段编码抗原蛋白的完整mRNA,包括5’和3’的未翻译区,5’端有帽结构(UTRs,一种调控序列),3’有Poly(A)尾,用于稳定mRNA和促进转录;同时mRNA还有多种碱基修饰来提高mRNA的稳定性,最后利用纳米脂质体等递送技术将mRNA递送至细胞内,从而翻译抗原蛋白,引发免疫反应。

安全性
mRNA并不会感染或者整合进基因组,因此不会带来感染或突变的风险。
有效性
有多种修饰方式能够使mRNA更佳稳定,翻译效率更高;同时递送方式的发展能够使mRNA快速递送到细胞内从而发挥功能。
生产便捷性
现在的体外转录技术能够非常快速、廉价地大规模生产RNA疫苗,相较于传统疫苗5-6个月的生产周期,mRNA疫苗有望在40天内完成疫苗样品的生产制备,因此有望更好地应对突发的传染病疫情。
mRNA 疫苗生产可分为两大块,“原料药”(mRNA)的生产和纯化,以及“制剂”(利用脂质微粒进行包封)阶段。原料药(mRNA)生产涉及 DNA 原液制备和 mRNA 原液的制备,mRNA 原液的制备(体外转录),是整个 mRNA 工艺流程中核心的步骤,所以mRNA 疫苗酶是最重要的原料,也是价值链最大的一块,预计10 亿剂mRNA疫苗将带来60 -70亿元的酶相关的需求。
T7 RNA 聚合酶、无机焦磷酸酶、Rnase Inhibitor、加帽酶、 2′O-甲基转移酶、Poly(A)聚合酶、 DNAase 等主要 7 种酶。
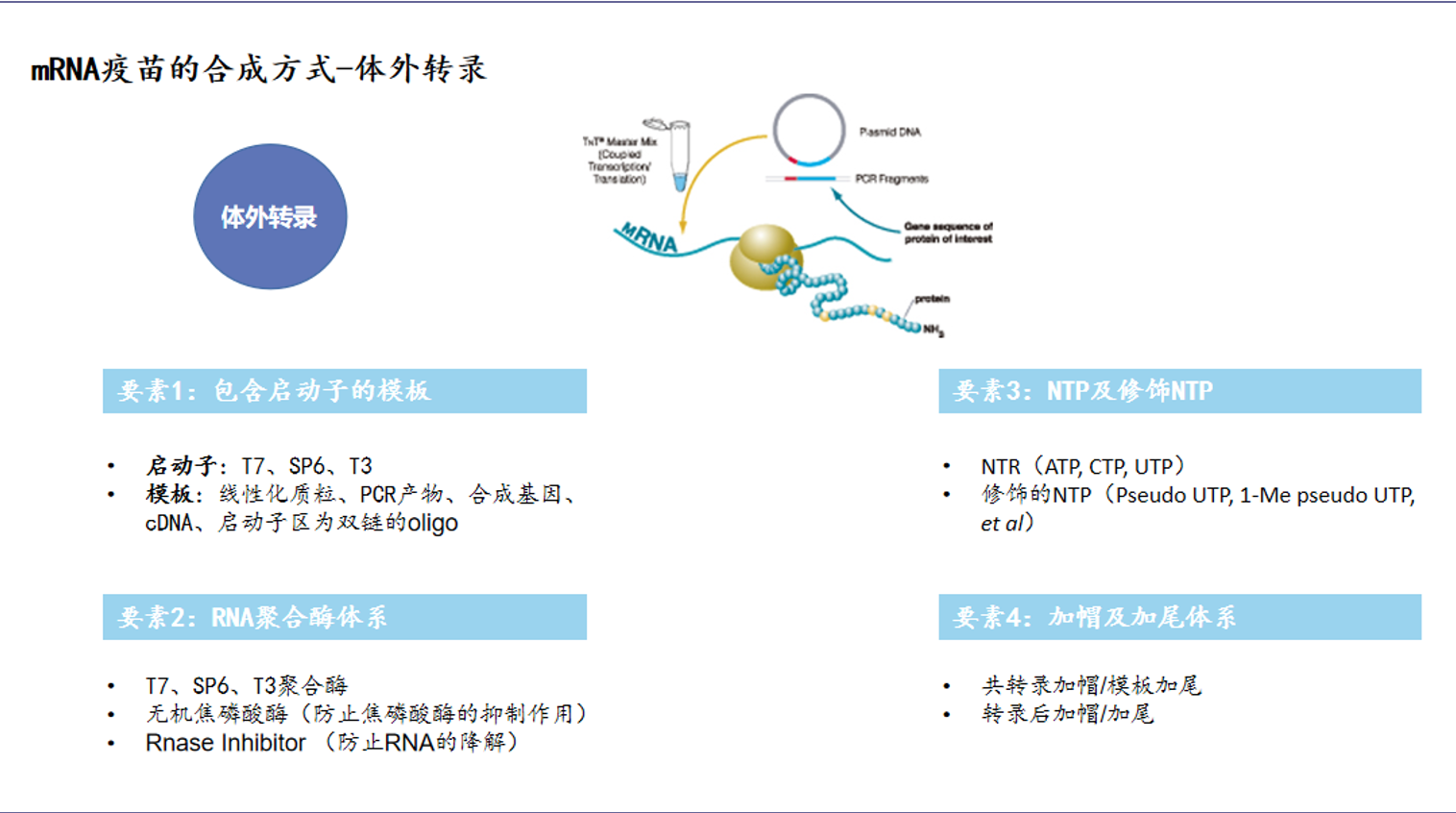
RNA 聚合酶是体外转录 mRNA 的关键酶。T3、T7和SP6 RNA聚合酶分别对T3、T7和SP6噬菌体启动子具有高度的特异性。将目的基因序列克隆到T7和SP6启动子下游的多克隆位点中,以克隆的DNA为模板体外合成相应的RNA。T7 RNA Polymerase(T7 RNA 聚合酶)高度特异识别T7启动子序列,以含有T7启动子序列的单链或双链DNA为模板,以核甘酸(NTP)为底物,合成与启动子下游的单链DNA互补的RNA。
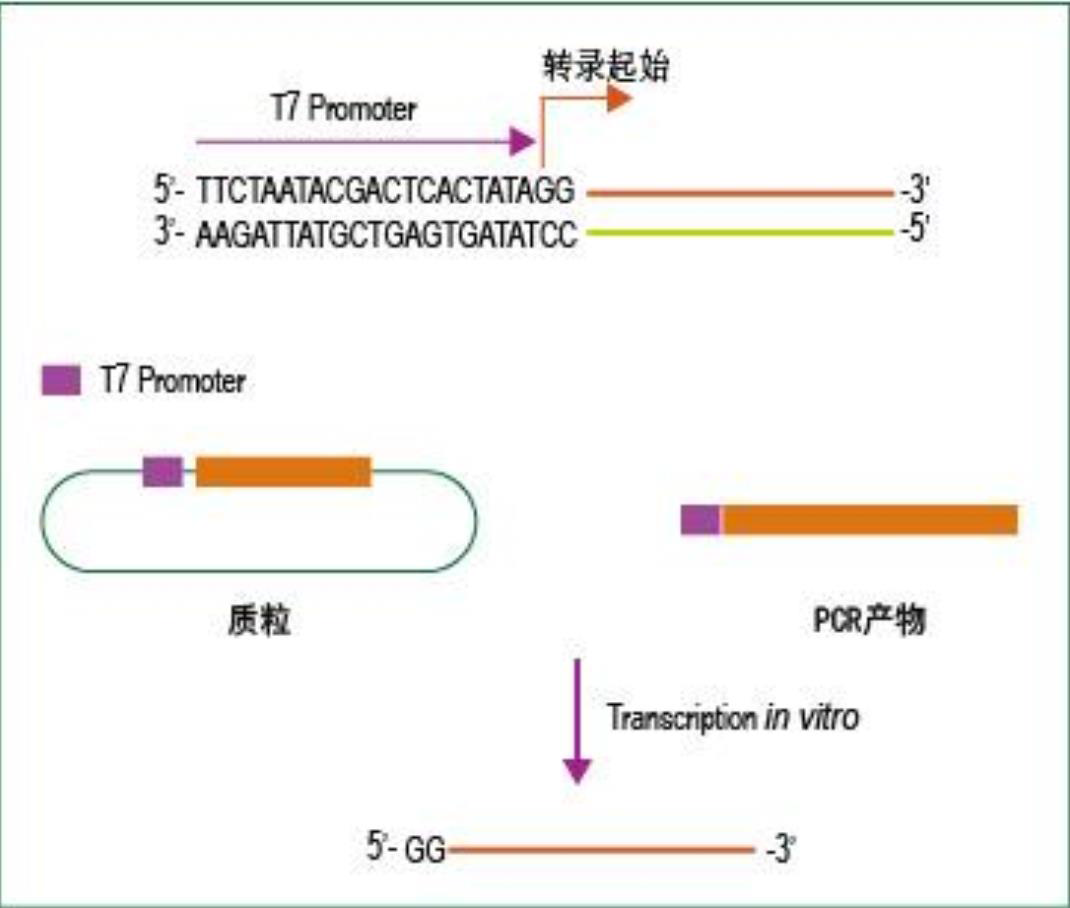
应用于制备放射标记的RNA探针合成,用于体外翻译的RNA合成,用于结构、加工和催化性能研究的RNA,合成RNA反义链,调控基因表达。
德奥平生物提供自主研发的
T7 RNA Polymerase(T7 RNA 聚合酶)
可批量订购
GMP车间生产
ISO13485严格质量控制
可应用于核酸药物、核酸疫苗的生产
欢迎订购:product@dia-up.com 18510836925、18610896066